अंगूठी मुद्रण

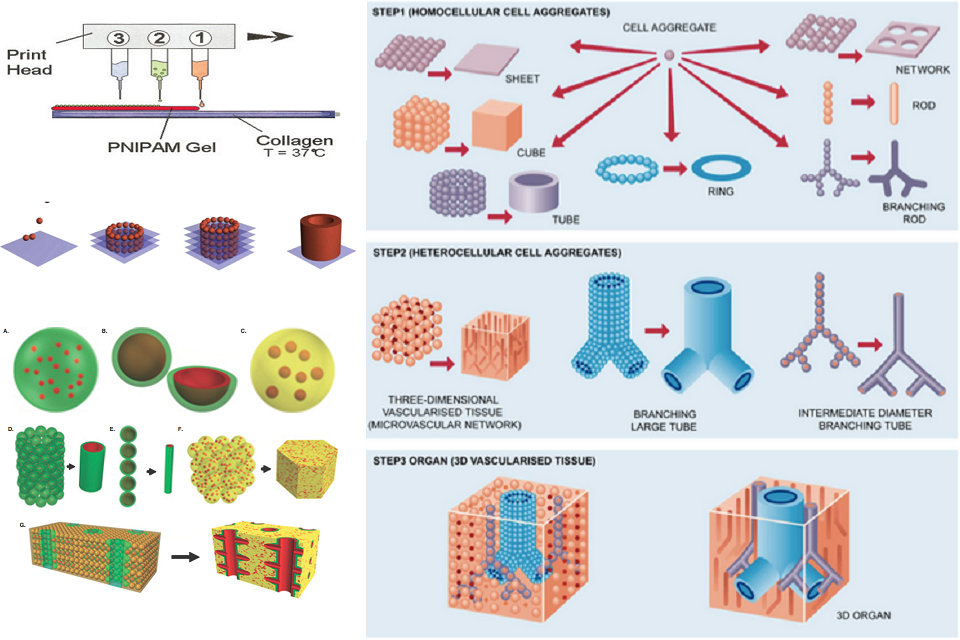
एक प्रिंट करने योग्य अंग एक कृत्रिम रूप से निर्मित डिवाइस है जो 3 डी प्रिंटिंग तकनीकों का उपयोग करके उत्पादित प्रतिस्थापन के लिए डिज़ाइन किया गया है। प्रिंट करने योग्य अंगों का प्राथमिक उद्देश्य प्रत्यारोपण में है। वर्तमान में अनुसंधान कृत्रिम दिल, गुर्दे, और जिगर संरचनाओं के साथ-साथ अन्य प्रमुख अंगों पर भी आयोजित किया जा रहा है। हृदय के रूप में अधिक जटिल अंगों के लिए, हृदय वाल्व जैसे छोटे निर्माण भी अनुसंधान का विषय रहे हैं। कुछ मुद्रित अंग नैदानिक कार्यान्वयन के लिए कार्यक्षमता आवश्यकताओं के निकट आ रहे हैं, और मुख्य रूप से मूत्राशय जैसे खोखले संरचनाओं, साथ ही मूत्र ट्यूब जैसे संवहनी संरचनाएं शामिल हैं।
3 डी प्रिंटिंग एक सेल मचान बनाने के लिए एक विशेष अंग संरचना के परत-दर-परत निर्माण के लिए अनुमति देता है। इसके बाद सेल बीजिंग की प्रक्रिया हो सकती है, जिसमें ब्याज की कोशिकाएं सीधे मचान संरचना पर पिपेट की जाती हैं। इसके अतिरिक्त, बाद में बीजिंग करने की बजाय, प्रिंट करने योग्य सामग्री में कोशिकाओं को एकीकृत करने की प्रक्रिया का पता लगाया गया है।
संशोधित इंकजेट प्रिंटर का उपयोग त्रि-आयामी जैविक ऊतक के उत्पादन के लिए किया गया है। प्रिंटर कारतूस जीवित कोशिकाओं और एक स्मार्ट जेल के निलंबन से भरे हुए हैं, बाद में संरचना प्रदान करने के लिए उपयोग किया जाता है। स्मार्ट जेल और जीवित कोशिकाओं के वैकल्पिक पैटर्न मानक प्रिंट नोजल का उपयोग करके मुद्रित होते हैं, कोशिकाएं अंततः ऊतक बनाने के लिए एक साथ फ्यूजिंग करती हैं। पूरा होने पर, जेल ठंडा और धोया जाता है, केवल जीवित कोशिकाओं के पीछे छोड़ देता है।
इतिहास
सेलुलर निर्माण के उत्पादन के लिए 3 डी प्रिंटिंग पहली बार 2003 में पेश की गई थी, जब थॉमस बोलैंड का Clemson विश्वविद्यालय कोशिकाओं के लिए इंकजेट मुद्रण के उपयोग पेटेंट। इस प्रक्रिया ने कोशिकाओं के जमाव के लिए एक सब्सट्रेट पर रखे संगठित 3 डी मैट्रिस में एक संशोधित स्पॉटिंग सिस्टम का उपयोग किया।
बोललैंड के शुरुआती निष्कर्षों के बाद से, जैविक संरचनाओं की 3 डी प्रिंटिंग जिसे बायोप्रिंटिंग भी कहा जाता है, को सेल मैट्रिस के विपरीत ऊतक और अंग संरचनाओं के उत्पादन को शामिल करने के लिए और विकसित किया गया है। इसके अतिरिक्त, प्रिंटिंग के लिए अधिक तकनीकें, जैसे एक्सट्रूज़न बायोप्रिंटिंग, का शोध किया गया है और बाद में उत्पादन के साधन के रूप में पेश किया गया है।
अंगूर मुद्रण को दाता अंगों की वैश्विक कमी के संभावित समाधान के रूप में संपर्क किया गया है। क्लिनिकल सेटिंग में सफलतापूर्वक मुद्रित और कार्यान्वित किए गए अंग या तो फ्लैट होते हैं, जैसे त्वचा, संवहनी, जैसे रक्त वाहिकाओं, या खोखले, जैसे मूत्राशय। जब प्रत्यारोपण के लिए कृत्रिम अंग तैयार किए जाते हैं, तो उन्हें अक्सर प्राप्तकर्ता की अपनी कोशिकाओं के साथ उत्पादित किया जाता है।
अधिक जटिल अंग, अर्थात् ठोस सेलुलर संरचनाओं वाले, अनुसंधान से गुज़र रहे हैं; इन अंगों में दिल, पैनक्रिया और गुर्दे शामिल हैं। अनुमान है कि ऐसे अंगों को व्यावहारिक चिकित्सा उपचार के रूप में पेश किया जा सकता है। 2013 में, कंपनी ऑर्गनोवो ने 3 डी बायोप्रिंटिंग का उपयोग करके एक मानव यकृत का उत्पादन किया, हालांकि यह प्रत्यारोपण के लिए उपयुक्त नहीं है, और मुख्य रूप से दवा परीक्षण के लिए एक माध्यम के रूप में उपयोग किया जाता है।
दृष्टिकोण
शोधकर्ताओं ने जीवित सिंथेटिक अंगों के उत्पादन के लिए विभिन्न दृष्टिकोण विकसित किए हैं। 3 डी बायो-प्रिंटिंग तीन मुख्य दृष्टिकोणों पर आधारित है: बायोमिमिरी, स्वायत्त स्व-असेंबली और मिनी ऊतक ब्लॉक का निर्माण।
बायोमिमिक्री
बायो-प्रिंटिंग के लिए पहला दृष्टिकोण बायोमिमिरी कहा जाता है। इस दृष्टिकोण का मुख्य उद्देश्य प्राकृतिक संरचनाओं के समान संरचनाएं बनाना है। बायोमिमिरी को अंगों, ऊतकों और ऊतकों के आकार, फ्रेम और सूक्ष्म पर्यावरण के दोहराव की आवश्यकता होती है। बायो-प्रिंटिंग में बायोमिमिरी अनुप्रयोग में अंगुलियों और अंगों के बाह्य कोशिकाओं की समान प्रति शामिल होती है। इस दृष्टिकोण को सफल होने के लिए, एक माइक्रोन पैमाने पर ऊतक प्रतिकृति की आवश्यकता है। परिशुद्धता की इस डिग्री में सूक्ष्मजीव, जैविक बलों की प्रकृति, कोशिकाओं का सटीक संगठन, घुलनशीलता कारक और बाह्य कोशिकीय मैट्रिक्स की संरचना और संरचना को समझना शामिल है।
स्व विधानसभा
बायो-प्रिंटिंग में इस्तेमाल किया जाने वाला दूसरा दृष्टिकोण स्वायत्त आत्म-असेंबली है। यह दृष्टिकोण भ्रूण अंग विकसित करने की प्राकृतिक शारीरिक प्रक्रिया पर निर्भर करता है। जब कोशिकाएं अपने प्रारंभिक विकास चरण में होती हैं, तो वे अपना स्वयं का बाह्य कोशिकीय मैट्रिक्स बिल्डिंग ब्लॉक बनाते हैं, और अपने स्वयं के उचित सेल सिग्नलिंग का उत्पादन करते हैं और अपेक्षित जैविक कार्यों को प्रदान करने के लिए आवश्यक लेआउट और माइक्रोआर्किटेक्चर लेते हैं। स्वायत्त आत्म-असेंबली में भ्रूण में ऊतकों और अंगों के विकास की प्रक्रियाओं के ज्ञान की आवश्यकता होती है। स्वायत्त आत्म-असेंबली सेल क्षमताओं पर हिस्टोजेनेसिस के मौलिक भवन ब्लॉक के रूप में निर्भर करती है। इसलिए इस तकनीक को भ्रूण ऊतक के विकास के साथ-साथ सूक्ष्म वातावरण में ऊतक बढ़ने के तंत्र की पूरी तरह से समझने की आवश्यकता होती है।
मिनी कपड़े
बायो-प्रिंटिंग का तीसरा दृष्टिकोण बायोमेमेटिक और स्व-असेंबली दृष्टिकोण दोनों का संयोजन है। इस तकनीक को “मिनी-ऊतक” के रूप में जाना जाता है। अंग और ऊतक बहुत छोटे कार्यात्मक घटकों से बने होते हैं। मिनी-फैब्रिक दृष्टिकोण इन छोटे टुकड़ों को लेना और उन्हें बड़ी संरचना में व्यवस्थित करना है। यह दृष्टिकोण दो अलग-अलग रणनीतियों का उपयोग करता है। पहली रणनीति एक गाइड के रूप में प्राकृतिक पैटर्न का उपयोग करके बड़े पैमाने पर कपड़े में स्वयं-संयोजन सेल क्षेत्रों का उपयोग करना है। दूसरी रणनीति सटीक प्रजनन और कपड़े की उच्च गुणवत्ता विकसित करना है और उन्हें बड़े कार्यात्मक कपड़े में स्केल करने के लिए स्वचालित रूप से माउंट करने की अनुमति है। एक जटिल त्रि-आयामी जैविक संरचना को मुद्रित करने के लिए इन रणनीतियों का मिश्रण आवश्यक है।
समय बचाने, लागत कम करने और मरीजों और मरीजों के लिए नए अवसर बनाने के लिए दवा और शल्य चिकित्सा प्रक्रियाओं को आगे बढ़ाने के लिए एनबीआईसी प्रौद्योगिकियों (नैनो, जैव, सूचना और संज्ञानात्मक) के लिए अंगों की छपाई की बड़ी संभावना है। स्वास्थ्य व्यवसायी।
3 डी प्रिंटिंग तकनीकें
कृत्रिम अंगों के निर्माण के लिए 3 डी प्रिंटिंग जैविक इंजीनियरिंग में अध्ययन का एक प्रमुख विषय रहा है। चूंकि 3 डी प्रिंटिंग द्वारा शुरू की गई तेजी से विनिर्माण तकनीकें तेजी से कुशल बनती हैं, कृत्रिम अंग संश्लेषण में उनकी प्रयोज्यता अधिक स्पष्ट हो गई है। 3 डी प्रिंटिंग के कुछ प्राथमिक लाभ बड़े पैमाने पर उत्पादक मचान संरचनाओं की क्षमता में, साथ ही साथ मचान उत्पादों में उच्चतम शारीरिक परिशुद्धता की क्षमता में हैं। यह संरचनाओं के निर्माण की अनुमति देता है जो प्राकृतिक अंग या ऊतक संरचना के सूक्ष्म संरचना के समान प्रभावी ढंग से मिलते हैं।
3 डी प्रिंटिंग का उपयोग करके ऑर्गन प्रिंटिंग विभिन्न तकनीकों का उपयोग करके आयोजित की जा सकती है, जिनमें से प्रत्येक विशिष्ट फायदे प्रदान करता है जो विशेष प्रकार के अंग उत्पादन के लिए उपयुक्त हो सकते हैं। अंग प्रिंटिंग के सबसे प्रमुख प्रकारों में से दो ड्रॉप-आधारित बायोप्रिंटिंग और एक्सट्रूज़न बायोप्रिंटिंग हैं। कई अन्य मौजूद हैं, हालांकि आमतौर पर उपयोग नहीं किए जाते हैं, या अभी भी विकास में हैं।
ड्रॉप-आधारित बायोप्रिंटिंग (इंकजेट)
ड्रॉप-आधारित बायोप्रिंटिंग एक निर्दिष्ट सामग्री की व्यक्तिगत बूंदों का उपयोग करके सेलुलर संरचनाएं बनाती है, जिसे कई बार सेल लाइन के साथ जोड़ा गया है। सब्सट्रेट सतह के संपर्क में, प्रत्येक बूंद बहुलक होने लगती है, जिससे बड़ी बूंदें बनती हैं क्योंकि अलग-अलग बूंदों को जोड़ना शुरू होता है। पॉलिमरराइजेशन सब्सट्रेट पर कैल्शियम आयनों की उपस्थिति से प्रेरित होता है, जो तरल पदार्थ बायोइंक में फैलता है और ठोस जेल के गठन की अनुमति देता है। ड्रॉप-आधारित बायोप्रिंटिंग का उपयोग आमतौर पर इसकी कुशल गति के कारण किया जाता है, हालांकि यह पहलू इसे अधिक जटिल अंग संरचनाओं के लिए कम उपयुक्त बनाता है।
एक्सट्रूज़न बायोप्रिंटिंग
एक्सट्रूज़न बायोप्रिंटिंग में एक विशेष प्रिंटिंग सामग्री और एक एक्सट्रूडर से सेल लाइन, एक प्रकार का मोबाइल प्रिंट हेड का निरंतर जमाव शामिल होता है। यह सामग्री या सेल जमावट के लिए एक अधिक नियंत्रित और gentler प्रक्रिया हो जाता है, और 3 डी ऊतक या अंग संरचनाओं के निर्माण में अधिक सेल घनत्व का उपयोग करने की अनुमति देता है। हालांकि, इस तरह के लाभ इस तकनीक से जुड़ी धीमी प्रिंटिंग गति से वापस सेट किए जाते हैं। एक्सट्रूज़न बायोप्रिंटिंग अक्सर यूवी प्रकाश के साथ मिलकर बनती है, जो अधिक स्थिर, एकीकृत निर्माण के लिए मुद्रित सामग्री को फोटोपॉलिमराइज करती है।
मुद्रण सामग्री
3 डी प्रिंटिंग के लिए सामग्री आमतौर पर अल्जीनेट या फाइब्रिन पॉलिमर होते हैं जिन्हें सेलुलर आसंजन अणुओं के साथ एकीकृत किया गया है, जो कोशिकाओं के भौतिक अनुलग्नक का समर्थन करते हैं। ऐसे बहुलक विशेष रूप से संरचनात्मक स्थिरता बनाए रखने के लिए डिजाइन किए जाते हैं और सेलुलर एकीकरण के लिए ग्रहणशील होते हैं। “बायोइंक” शब्द का उपयोग उन सामग्रियों के व्यापक वर्गीकरण के रूप में किया गया है जो 3 डी बायोप्रिंटिंग के अनुकूल हैं।
प्रिंटिंग सामग्री को मानदंडों का एक व्यापक स्पेक्ट्रम फिट करना चाहिए, जो कि सबसे प्रमुख जैव-अनुकूलता है। 3 डी मुद्रित सामग्रियों द्वारा गठित परिणामी मचान सेल प्रसार के लिए शारीरिक रूप से और रासायनिक रूप से उपयुक्त होना चाहिए। बायोडिग्रेडेबिलिटी एक और महत्वपूर्ण कारक है, और बीमा करता है कि कृत्रिम रूप से गठित संरचना को सफल प्रत्यारोपण पर तोड़ दिया जा सकता है, जिसे पूरी तरह से प्राकृतिक सेलुलर संरचना द्वारा प्रतिस्थापित किया जा सकता है। 3 डी प्रिंटिंग की प्रकृति के कारण, उपयोग की जाने वाली सामग्री को अनुकूलन और अनुकूलनीय होना चाहिए, जो कि सेल प्रकारों और संरचनात्मक अनुरूपताओं की विस्तृत श्रृंखला के अनुकूल है।
हाइड्रोगेल एल्गिनेट्स अंग मुद्रण शोध में सबसे अधिक उपयोग की जाने वाली सामग्रियों में से एक के रूप में उभरे हैं, क्योंकि वे अत्यधिक अनुकूलन योग्य हैं, और प्राकृतिक ऊतक की कुछ यांत्रिक और जैविक गुणों की विशेषता को अनुकरण करने के लिए ठीक-ठीक किया जा सकता है। विशिष्ट जरूरतों के अनुरूप बनने के लिए हाइड्रोगल्स की क्षमता उन्हें एक अनुकूलनीय मचान सामग्री के रूप में उपयोग करने की अनुमति देती है, जो विभिन्न ऊतक या अंग संरचनाओं और शारीरिक स्थितियों के लिए उपयुक्त होती है। एल्गिनेट के उपयोग में एक बड़ी चुनौती इसकी स्थिरता और धीमी गिरावट है, जिससे कृत्रिम जेल मचान को तोड़ना मुश्किल हो जाता है और प्रत्यारोपित कोशिकाओं के अपने बाह्य कोशिका मैट्रिक्स के साथ बदल दिया जाता है। एक्सगिनेट हाइड्रोगेल जो एक्सट्रूज़न प्रिंटिंग के लिए उपयुक्त है अक्सर भी कम संरचनात्मक और यांत्रिक रूप से ध्वनि होता है; हालांकि, अधिक स्थिरता प्रदान करने के लिए, इस समस्या को अन्य बायोपॉलिमर्स, जैसे नैनोसेल्यूलोस के निगमन द्वारा मध्यस्थता में मध्यस्थता दी जा सकती है। Alginate या मिश्रित बहुलक बायोइंक के गुण ट्यून करने योग्य हैं और विभिन्न अनुप्रयोगों और अंगों के प्रकार के लिए बदला जा सकता है।
अंग संरचनाएं
जबकि अंग मुद्रण की कई तकनीकी चुनौतियों को 3 डी बायोप्रिंटिंग के अन्य अनुप्रयोगों के साथ साझा किया जाता है, कुछ अंग-विशिष्ट संरचनात्मक तत्व होते हैं जिन्हें एक प्रत्यारोपित मुद्रित अंग के सफल निर्माण के लिए संबोधित किया जाना चाहिए।
vascularization
एक मुद्रित अंग में कोशिकाओं को पोषक तत्वों और ऑक्सीजन का स्थानांतरण अपने कार्य के लिए आवश्यक है। मोटाई में एक मिलीमीटर से भी कम के बहुत छोटे या पतले ऊतकों में, कोशिकाएं प्रसार के माध्यम से पोषक तत्व प्राप्त कर सकती हैं। हालांकि, बड़े अंगों को ऊतक के अंदर गहरे कोशिकाओं में पोषक तत्वों के परिवहन की आवश्यकता होती है, जिसके लिए ऊतक संवहनीकृत होता है, और इस प्रकार ऑक्सीजन और सेल अपशिष्ट जैसे कार्गो के आदान-प्रदान के लिए रक्त प्राप्त करने में सक्षम होता है। शुरुआती अंग मुद्रण तकनीकों ने ठोस ऊतकों का निर्माण किया जो संवहनीकरण में असमर्थ थे, या केवल धीरे-धीरे संवहनीकृत होते थे क्योंकि होस्ट रक्त वाहिकाओं ने प्रत्यारोपण में प्रवेश किया था, जिससे ऊतक के अंदर नेक्रोसिस जैसे मुद्दों को जन्म दिया गया था जो एक प्रत्यारोपण प्राप्तकर्ता के स्वास्थ्य और सफल वसूली को खतरे में डाल सकते हैं। हाल ही में विकसित तकनीकें मुद्रित अंगों को एक अधिक जटिल 3 डी संरचना के साथ बनाने की अनुमति देती हैं, जिसमें पूर्ववर्ती आंतरिक वास्कुलचर भी शामिल है, जो मेजबान परिसंचरण तंत्र में प्रत्यारोपण के तेज़ एकीकरण की अनुमति देता है। वर्तमान में विकास के तहत संवहनी तंत्र बनाने के लिए कई तकनीकें हैं। एक विधि जहाजों की अलग निकासी मुद्रण है जिसे तब बड़े ऊतक में शामिल किया जाता है। एक अन्य विधि बलिदान प्रिंटिंग है, जिसमें पूरे ऊतक एक बार में मुद्रित होते हैं, और एक विघटनकारी या अन्यथा हटाने योग्य बायोइंक का उपयोग जहाजों के इंटीरियर को बनाने के लिए किया जाता है। एक बार यह बलिदान मचान हटा दिया जाता है, आमतौर पर एक रासायनिक या थर्मल विधि द्वारा, शेष ऊतक में एक संवहनी पैटर्न होता है।
सेल स्रोत
एक पूर्ण अंग के निर्माण के लिए अक्सर अलग-अलग प्रकार के विभिन्न प्रकार के प्रकारों को शामिल करने की आवश्यकता होती है, जो विशिष्ट और पैटर्न वाले तरीके से व्यवस्थित होते हैं। पारंपरिक प्रत्यारोपण की तुलना में 3 डी मुद्रित अंगों का एक लाभ, नए अंग को बनाने के लिए रोगी से प्राप्त कोशिकाओं का उपयोग करने की क्षमता है। यह प्रत्यारोपण अस्वीकृति की संभावना को काफी कम करता है, और प्रत्यारोपण के बाद immunosuppressive दवाओं की आवश्यकता को हटा सकता है, जो प्रत्यारोपण के स्वास्थ्य जोखिम को कम करेगा। हालांकि, चूंकि सभी आवश्यक सेल प्रकारों को इकट्ठा करना हमेशा संभव नहीं होता है, इसलिए वयस्क स्टेम कोशिकाओं को इकट्ठा करना या एकत्रित ऊतक में प्लुरिपोटेंसी उत्पन्न करना आवश्यक हो सकता है। इसमें संसाधन-केंद्रित सेल वृद्धि और भेदभाव शामिल है और संभावित स्वास्थ्य जोखिमों के अपने सेट के साथ आता है, क्योंकि एक मुद्रित अंग में सेल प्रसार शरीर के बाहर होता है और विकास कारकों के बाहरी अनुप्रयोग की आवश्यकता होती है। हालांकि, अलग-अलग संरचनाओं में स्वयं को व्यवस्थित करने के लिए कुछ ऊतकों की क्षमता एक साथ ऊतकों का निर्माण करने और अलग-अलग सेल आबादी बनाने का एक तरीका प्रदान कर सकती है, जिससे अंग मुद्रण की प्रभावकारिता और कार्यक्षमता में सुधार होता है।