L’économie du méthanol est une économie future suggérée dans laquelle le méthanol et l’éther diméthylique remplacent les combustibles fossiles comme moyen de stockage de l’énergie, de carburant pour les transports terrestres et de matière première pour les hydrocarbures synthétiques et leurs produits. Il offre une alternative à l’économie de l’hydrogène ou de l’éthanol proposée.
Dans les années 1990, George A. Olah, lauréat du prix Nobel, prônait une économie du méthanol.En 2006, GK Surya Prakash et Alain Goeppert, ses deux coauteurs, ont publié un résumé de l’état des combustibles fossiles et des sources d’énergie de remplacement, y compris de leur disponibilité et de leurs limites, avant de proposer une économie du méthanol.
Le méthanol peut être produit à partir d’une grande variété de sources, notamment des combustibles fossiles encore abondants (gaz naturel, charbon, schistes bitumineux, sables bitumineux, etc.), ainsi que des produits agricoles et des déchets municipaux, du bois et de la biomasse variée. Il peut également être fabriqué à partir de recyclage chimique du dioxyde de carbone.
introduction
En 2005, le prix Nobel George A. Olah a appelé à la création d’une économie du méthanol dans l’essai Au-delà du pétrole et du gaz: l’économie du méthanol. En 2006, avec deux autres co-auteurs, a publié un livre sur le sujet. les auteurs résument l’état des sources de combustibles fossiles et d’autres sources d’énergie de remplacement, leur disponibilité et leurs limites avant de suggérer l’expérimentation de l’économie dite du méthanol.
Le méthanol est un carburant qui peut être utilisé à la fois pour les moteurs thermiques et pour les piles à combustible. Grâce à son bon indice d’octane, il peut être utilisé directement comme carburant dans les voitures (y compris les voitures hybrides et les modèles enfichables) avec différents types de moteurs à combustion interne déjà utilisés. Le méthanol peut également être utilisé dans la pile à combustible, directement, dans les cellules DMFC ou indirectement, après sa transformation en hydrogène par reformage.
Dans des conditions normales, le méthanol est un liquide qui permet de le stocker, de le transporter et de le distribuer facilement, comme pour l’essence et le diesel. Chimiquement, il peut également être rapidement transformé par déshydratation en diméthyléther, un substitut du diesel dont l’indice de cétane est 55.
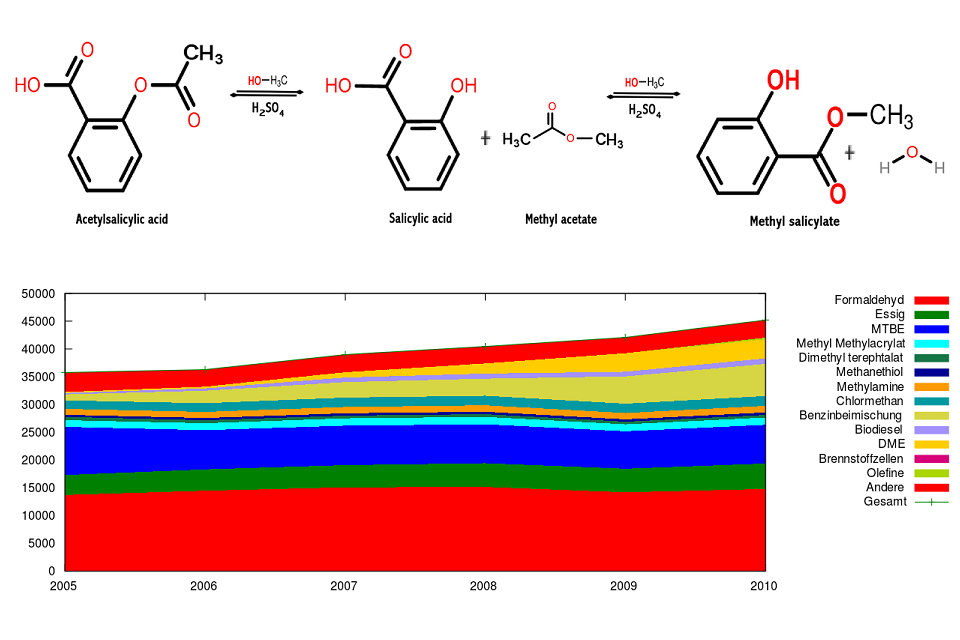
Dans les années 2000, le méthanol est utilisé à grande échelle (environ 37 millions de tonnes par an) en tant que brique chimique élémentaire pour la fabrication de nombreux produits chimiques complexes et de matériaux polymères. En outre, il peut être facilement converti par le procédé « du méthanol en oléfine » (MTO) dans l’éthylène et le propylène, des hydrocarbures insaturés pouvant être utilisés pour produire des hydrocarbures synthétiques de poids moléculaire plus élevé et d’autres dérivés de ceux-ci, généralement obtenus à partir de pétrole et de carburants. gaz naturel.
Sources de méthanol
Le méthanol peut être efficacement produit à partir d’une grande variété de sources, y compris certains types de combustibles fossiles très abondants (gaz naturel, charbon, schistes bitumineux, sable bitumineux, etc.), mais également à partir de déchets agricoles et de déchets urbains différenciés, du bois et de divers types de biomasse.
Recyclage du dioxyde de carbone
Une hypothèse beaucoup plus radicale consiste à obtenir du méthanol à partir du recyclage chimique du dioxyde de carbone. Au départ, la source principale pourrait être les émissions riches en CO 2 provenant de centrales électriques utilisant des combustibles fossiles ou les rejets de cimenteries et d’autres usines. À plus long terme, compte tenu de la diminution des ressources en combustibles fossiles et des effets de leur utilisation sur l’atmosphère de la Terre, même la faible concentration de CO 2 naturel pourrait être capturée et recyclée pour obtenir du méthanol: elle contribuerait ainsi à le même cycle naturel de photosynthèse. De nouvelles substances absorbantes plus efficaces sont en cours de développement, capables de capter le CO 2 atmosphérique, qui dans certains cas imite l’action de plantes vivantes. Le recyclage chimique du CO 2 pour obtenir de nouveaux combustibles et matériaux pourrait alors devenir possible et durable, ce qui rendrait ces « carburants au carbone non fossile » renouvelables sur une période comparable à la durée de vie. En Islande, en 2011/2012, une production de deux millions de litres de méthanol par an a déjà commencé avec ce système.
Les usages
Carburant
Le méthanol est un carburant pour les moteurs thermiques et les piles à combustible. En raison de son indice d’octane élevé, il peut être utilisé directement comme carburant dans les voitures polycarburant (y compris les véhicules hybrides et hybrides rechargeables) utilisant des moteurs à combustion interne (ICE) existants. Le méthanol peut également être brûlé dans d’autres types de moteurs ou pour fournir de la chaleur lorsque d’autres combustibles liquides sont utilisés. Les piles à combustible peuvent utiliser le méthanol directement dans les piles à combustible à méthanol direct (DMFC) ou indirectement (après conversion en hydrogène par reformage).
Dans les moteurs à combustion interne (ICE)
Le méthanol a un indice d’octane élevé (RON de 107 et MON de 92), ce qui en fait un substitut adéquat à l’essence. Il a une vitesse de flamme plus élevée que l’essence, ce qui conduit à un rendement supérieur ainsi qu’à une chaleur de vaporisation latente plus grande (3,7 fois supérieure à celle de l’essence), ce qui implique que la chaleur générée par le moteur peut être évacuée plus efficacement, ce qui permet d’utiliser de l’air. moteurs refroidis. De plus, le méthanol brûle, polluant moins que l’essence et est plus sûr en cas d’incendie. Cependant, le méthanol ne contient que la moitié du contenu énergétique en volume par rapport à l’essence (8 600 BTU / livre).
Dans les moteurs à allumage par compression (moteur diesel)
Le méthanol en soi est un mauvais substitut pour les carburants diesel. Mais, à cause de la déshydratation chimique, le méthanol peut être transformé en diméthyléther (DME), qui est plutôt un bon carburant diesel avec un indice de cétane de 55-60, meilleur que l’indice de cétane 45-55 du diesel ordinaire. Par rapport aux carburants diesel, le DME émet beaucoup moins de particules, de NO x et de CO et n’émet aucun type de dioxyde de soufre ni de dioxyde de soufre (SO x). Le méthanol est également utilisé pour produire du biodiesel par la transestérification d’huiles végétales.
Dans les moteurs avancés ou dans les piles à combustible alimentées au méthanol
L’utilisation de méthanol et d’éther-diméthyle peut être combinée aux technologies de moteurs hybrides et de voitures électriques, de manière à obtenir un kilométrage plus important (kilomètres par litre) et des émissions plus faibles. Ces combustibles peuvent être utilisés à la fois dans les piles à combustible et les catalyseurs qui procèdent au reformage en obtenant de l’hydrogène pour alimenter la pile à combustible ou en « brûlant » directement du méthanol dans des piles à combustible à méthanol direct.
Pour la production d’électricité
Le méthanol et le DME peuvent être utilisés dans les turbines à gaz pour générer de l’électricité. Les modèles de pile à combustible actuellement très coûteux (PAFC, MCFC, SOFC) peuvent être utilisés pour la production d’électricité, en particulier dans les environnements où un faible bruit est requis, en plus d’une faible production de chaleur, tels que les hôpitaux; ou un très faible poids de la plante, comme dans les véhicules de transport aérien ou spatial.
Comme combustible domestique
Le méthanol et le DME peuvent être utilisés dans les bâtiments commerciaux et les maisons pour générer de la chaleur et / ou de l’électricité. Le DME peut être utilisé dans les cuisinières à gaz / cuisines commerciales sans modifications majeures. Dans les pays en développement, le méthanol pourrait être utilisé comme carburant pour la cuisine, car il brûle beaucoup plus propre que le bois (moins de nanoparticules et de CO), ce qui atténue ainsi certains des problèmes liés à la pollution domestique. mélangés avec de l’essence, du diesel ou des colorants-adultérants, afin d’éviter toute fraude éventuelle, ainsi que l’utilisation mortelle en tant qu’additif dans les boissons, un événement survenu en Italie avec l’arnaque au vin au méthanol.
Elément de base pour la chimie et les matériaux polymères
Actuellement, le méthanol est largement utilisé à grande échelle comme matériau de base pour la production de divers produits chimiques et autres produits tels que les polymères plastiques. Avec le processus connu sous le nom de « méthanol en essence » (MTG), le méthanol peut être transformé en essence. En utilisant le procédé « méthanol en oléfine » (MTO), le méthanol peut être converti en éthylène et en propylène alcènes, les deux produits chimiques fabriqués en plus grande quantité par l’industrie pétrochimique. Ce sont des éléments de base importants pour la production de polymères essentiels (LDPE, HDPE, PP) et d’autres intermédiaires chimiques actuellement produits à partir de dérivés du pétrole. Leur production à partir de méthanol pourrait donc réduire la dépendance au pétrole. Cela permettra également de continuer à produire ces produits chimiques et plastiques de base, même après la fin des dépôts de combustibles fossiles.
Matière première
Le méthanol est déjà utilisé aujourd’hui à grande échelle pour produire divers produits chimiques. La demande mondiale de méthanol en tant que matière première chimique a atteint environ 42 millions de tonnes métriques par an à partir de 2015. Le processus de transformation du méthanol en essence (MTG) permet de le transformer en essence. En utilisant le procédé de méthanol à oléfine (MTO), le méthanol peut également être converti en éthylène et en propylène, les deux produits chimiques produits en plus grande quantité par l’industrie pétrochimique. Ce sont des éléments de base importants pour la production de polymères essentiels (LDPE, HDPE, PP) et, à l’instar d’autres intermédiaires chimiques, ils sont actuellement produits principalement à partir de matières premières pétrolières. Leur production à partir de méthanol pourrait donc réduire notre dépendance au pétrole. Cela permettrait également de continuer à produire ces produits chimiques lorsque les réserves de combustibles fossiles seront épuisées.
Production
Aujourd’hui, la majeure partie du méthanol est produite à partir de méthane issu de gaz de synthèse.Trinité-et-Tobago est actuellement le plus grand exportateur de méthanol au monde, principalement aux États-Unis. Le gaz naturel qui sert de matière première pour la production de méthanol provient des mêmes sources que les autres utilisations. Des ressources gazières non conventionnelles, telles que le méthane de houille, le gaz de sable et, éventuellement, les très importantes ressources d’hydrate de méthane présentes sur les plateaux continentaux des mers, ainsi que la toundra sibérienne et canadienne, pourraient également servir à fournir le gaz nécessaire.
La voie conventionnelle du méthane au méthanol passe par la production de gaz de synthèse par reformage à la vapeur combiné (ou non) avec une oxydation partielle. De nouvelles méthodes plus efficaces pour convertir le méthane en méthanol sont également mises au point. Ceux-ci inclus:
Oxydation du méthane avec des catalyseurs homogènes en milieu acide sulfurique
Bromation de méthane suivie d’une hydrolyse du bromométhane obtenu
Oxydation directe du méthane avec de l’oxygène
Conversion microbienne ou photochimique du méthane
Oxydation partielle du méthane avec piégeage du produit partiellement oxydé et extraction ultérieure sur zéolite à échange de fer et de cuivre (par exemple alpha-oxygène)
Toutes ces voies de synthèse émettent du dioxyde de carbone CO2, un gaz à effet de serre. Pour atténuer cela, le méthanol peut être fabriqué par des moyens minimisant les émissions de CO2. Une solution consiste à le produire à partir de gaz de synthèse obtenu par gazéification de biomasse. À cette fin, toute biomasse peut être utilisée, y compris le bois, les déchets de bois, l’herbe, les cultures agricoles et leurs sous-produits, les déchets d’animaux, les plantes aquatiques et les déchets municipaux. Il n’est pas nécessaire d’utiliser des cultures vivrières comme dans le cas de l’éthanol de maïs, de la canne à sucre et du blé.
Biomasse → Gaz de synthèse (CO, CO 2 , H 2 ) → CH 3 OH
Le méthanol peut être synthétisé à partir de carbone et d’hydrogène à partir de n’importe quelle source, y compris les combustibles fossiles et la biomasse encore disponibles. Le CO2 émis par les centrales électriques à combustibles fossiles et d’autres industries, voire même le CO2 contenu dans l’air, peut être une source de carbone. Il peut également être fabriqué à partir de recyclage chimique du dioxyde de carbone, ce que Carbon Recycling International a démontré avec sa première usine à l’échelle commerciale. Initialement, la source principale sera les gaz de combustion riches en CO2 des centrales électriques à combustible fossile ou les gaz d’échappement des usines de ciment et autres. Cependant, à plus long terme, compte tenu de la diminution des ressources en combustibles fossiles et des effets de leur utilisation sur l’atmosphère terrestre, même la faible concentration de CO2 atmosphérique pourrait être capturée et recyclée via le méthanol, complétant ainsi le cycle photosynthétique de la nature. De nouveaux absorbants efficaces pour capter le CO2 atmosphérique sont en cours de développement, imitant ainsi la capacité des plantes. Le recyclage chimique du CO2 dans de nouveaux carburants et matériaux pourrait ainsi devenir réalisable, ce qui les rendrait renouvelables à l’échelle de temps humaine.
Le méthanol peut également être produit à partir de CO2 par hydrogénation catalytique de CO2 avec H2 lorsque l’hydrogène a été obtenu par électrolyse de l’eau. C’est le processus utilisé par Carbon Recycling International d’Islande. Le méthanol peut également être produit par réduction électrochimique du CO2, si de l’énergie électrique est disponible. L’énergie nécessaire à ces réactions pour être neutre en carbone proviendrait de sources d’énergie renouvelables telles que l’énergie éolienne, l’hydroélectricité et l’énergie solaire ainsi que de l’énergie nucléaire. En fait, ils permettent tous de stocker de l’énergie libre dans du méthanol facilement transportable, qui est fabriqué immédiatement à partir d’hydrogène et de dioxyde de carbone, plutôt que de tenter de stocker de l’énergie dans de l’hydrogène libre.
CO 2 + 3H 2 → CH 3 OH + H 2 O
ou avec de l’énergie électrique
CO 2 + 5H 2 O + 6 e −1 → CH 3 OH + 6 HO −1
6 HO −1 → 3H 2 O + 3/2 O 2 + 6 e −1
Total:
CO 2 + 2H 2 O + énergie électrique → CH 3 OH + 3/2 O 2
Le CO2 nécessaire serait capté par les centrales électriques à combustible fossile et d’autres gaz de combustion industriels, y compris les cimenteries. Avec la diminution des ressources en combustibles fossiles et donc des émissions de CO2, le contenu de CO2 dans l’air pourrait également être utilisé. Compte tenu de la faible concentration de CO2 dans l’air (0,04%), des technologies améliorées et économiquement viables pour absorber le CO2 devront être développées. Pour cette raison, l’extraction du CO2 de l’eau pourrait être plus faisable en raison de ses concentrations plus élevées sous forme dissoute. Cela permettrait le recyclage chimique du CO2, imitant ainsi la photosynthèse de la nature.
Les avantages
Lors du processus de photosynthèse, les plantes vertes utilisent l’énergie du soleil pour fractionner l’eau en oxygène libre (qui est libéré) et en hydrogène libre. Plutôt que d’essayer de stocker l’hydrogène, les plantes capturent immédiatement le dioxyde de carbone de l’air afin de permettre à l’hydrogène de le réduire en combustibles stockables tels que les hydrocarbures (huiles végétales et terpènes) et les polyalcools (glycérol, sucres et amidons). Dans l’économie du méthanol, tout procédé produisant de manière similaire de l’hydrogène libre propose de l’utiliser immédiatement « de manière captive » pour réduire le dioxyde de carbone en méthanol, qui, comme les produits végétaux issus de la photosynthèse, présente de grands avantages en termes de stockage et de transport par rapport à l’hydrogène libre lui-même.
Le méthanol est un liquide dans des conditions normales, ce qui lui permet d’être stocké, transporté et distribué facilement, un peu comme l’essence et le carburant diesel. Il peut également être facilement transformé par déshydratation en diméthyléther, un substitut du carburant diesel ayant un indice de cétane de 55.
Comparaison avec l’hydrogène
Avantages de l’économie du méthanol par rapport à une économie de l’hydrogène:
Stockage efficace de volume d’énergie par rapport à l’hydrogène comprimé. Lorsque l’on prend en compte la cuve de confinement d’hydrogène, on peut également obtenir un avantage en termes de stockage d’énergie en poids. La densité d’énergie volumétrique du méthanol est considérablement plus élevée que celle de l’hydrogène liquide, en partie à cause de la faible densité de l’hydrogène liquide de 71 grammes / litre. Par conséquent, il y a en réalité plus d’hydrogène dans un litre de méthanol (99 grammes / litre) que dans un litre d’hydrogène liquide, et le méthanol n’a pas besoin de conteneur cryogénique maintenu à une température de -253 ° C.
Une infrastructure à l’hydrogène liquide coûterait très cher. Le méthanol peut utiliser l’infrastructure d’essence existante avec seulement des modifications limitées.
Peut être mélangé à de l’essence (par exemple dans M85, un mélange contenant 85% de méthanol et 15% d’essence).
Convivial. L’hydrogène est volatil et son confinement utilise des systèmes à haute pression ou cryogéniques.
Moins de pertes: l’hydrogène fuit plus facilement que le méthanol. La chaleur va évaporer l’hydrogène liquide, entraînant des pertes attendues pouvant atteindre 0,3% par jour dans les réservoirs de stockage. (Voir les réservoirs de stockage Chart Ferox Oxygène).
Comparaison avec l’éthanol
Peut être fabriqué à partir de tout matériau organique en utilisant une technologie éprouvée utilisant le gaz de synthèse. Il n’est pas nécessaire d’utiliser des cultures vivrières et de concurrencer la production alimentaire. La quantité de méthanol pouvant être générée à partir de la biomasse est bien supérieure à celle de l’éthanol.
Peut rivaliser avec l’éthanol et le compléter, sur un marché de l’énergie diversifié. Le méthanol obtenu à partir de combustibles fossiles a un prix inférieur à celui de l’éthanol.
Peut être mélangé à de l’essence comme l’éthanol. En 2007, la Chine a mélangé plus de 1 800 000 m3 (3 800 000 m3) de méthanol dans un carburant et introduira une norme de carburant au méthanol d’ici à la mi-2008. Le M85, un mélange de 85% de méthanol et de 15% d’essence, peut être utilisé comme l’E85 vendu dans certaines stations-service aujourd’hui.
Désavantages
Les coûts énergétiques élevés associés à la production et au transport d’hydrogène à l’extérieur du site.
Selon la matière première, la génération en elle-même peut ne pas être propre.
Actuellement générée à partir de gaz naturel, elle dépend encore de combustibles fossiles (bien que tout hydrocarbure combustible puisse être utilisé).
Densité énergétique (en poids ou en volume) la moitié de celle de l’essence et 24% de moins que l’éthanol
Manipulation
Si aucun inhibiteur n’est utilisé, le méthanol est corrosif pour certains métaux courants, notamment l’aluminium, le zinc et le manganèse. Certaines parties des systèmes d’admission de carburant du moteur sont en aluminium. Semblable à l’éthanol, un matériau compatible pour les réservoirs de carburant, le joint d’étanchéité et l’admission du moteur doit être utilisé.
Comme avec l’éthanol corrosif et hydrophile, les pipelines existants conçus pour les produits pétroliers ne peuvent pas traiter le méthanol. Ainsi, le méthanol nécessite une expédition à un coût énergétique plus élevé dans les camions et les trains, en attendant la construction d’une nouvelle infrastructure de pipeline ou la modernisation des pipelines existants pour le transport du méthanol.
Le méthanol, en tant qu’alcool, augmente la perméabilité de certains plastiques aux vapeurs de carburant (par exemple, le polyéthylène haute densité). Cette propriété du méthanol a le potentiel d’augmenter les émissions de composés organiques volatils (COV) du carburant, ce qui contribue à augmenter l’ozone troposphérique et éventuellement l’exposition humaine.
Faible volatilité par temps froid: les moteurs fonctionnant au méthanol pur peuvent être difficiles à démarrer et ils fonctionnent de manière inefficace jusqu’à ce qu’ils soient réchauffés. C’est pourquoi on utilise généralement un mélange contenant 85% de méthanol et 15% d’essence appelé M85.L’essence permet au moteur de démarrer même à des températures plus basses.
À l’exception des faibles niveaux d’exposition, le méthanol est toxique. Le méthanol est mortel lorsqu’il est ingéré en plus grande quantité (30 à 100 ml). Mais la plupart des carburants, y compris l’essence (120 à 300 ml) et le diesel, le sont également. L’essence contient également de petites quantités de nombreux composés connus pour être cancérigènes (par exemple le benzène). Le méthanol n’est pas un cancérigène, ni ne contient de carcinogènes. Cependant, le méthanol peut être métabolisé dans l’organisme en formaldéhyde, qui est à la fois toxique et cancérigène. Le méthanol est naturellement présent en petites quantités dans le corps humain et dans les fruits comestibles.
Le méthanol est un liquide: cela crée un plus grand risque d’incendie que l’hydrogène dans les espaces ouverts, car les fuites de méthanol ne se dissipent pas. Le méthanol brûle de manière invisible contrairement à l’essence. Comparativement à l’essence, le méthanol est beaucoup plus sûr. Il est plus difficile de s’enflammer et libère moins de chaleur quand il brûle. Les incendies au méthanol peuvent être éteints avec de l’eau ordinaire, alors que l’essence flotte sur l’eau et continue à brûler. L’EPA a estimé que le remplacement des carburants d’essence par du méthanol réduirait l’incidence des incendies liés aux carburants de 90%.
Le méthanol est soluble dans l’eau: libéré accidentellement, il peut subir un transport relativement rapide des eaux souterraines, entraînant une pollution des eaux souterraines, bien que ce risque n’ait pas été complètement étudié. Un rejet accidentel de méthanol dans l’environnement causerait cependant beaucoup moins de dégâts qu’un déversement comparable d’essence ou de pétrole brut.Contrairement à ces carburants, le méthanol est biodégradable et totalement soluble dans l’eau. Il serait rapidement dilué à une concentration suffisamment basse pour que le microorganisme puisse commencer sa biodégradation. Cet effet est déjà exploité dans les usines de traitement des eaux, où le méthanol est déjà utilisé pour la dénitrification et comme élément nutritif pour les bactéries.
Application
Le méthanol et ses dérivés, tels que le diméthyléther, peuvent ensuite être utilisés pour générer de l’électricité à la fois dans les moteurs à combustion interne classiques et comme combustible dans les piles à combustible au méthanol.
Le stockage, le transport et la distribution du méthanol, qui est liquide à la température ambiante, peuvent utiliser l’infrastructure et la technologie existantes. Les grandes distances entre consommateurs et producteurs d’énergies régénératives peuvent alors être efficacement comblées.La densité de stockage d’énergie est d’environ 50% de la densité de stockage de l’essence et du diesel.
L’Europe
En Islande, Carbon Recycling International exploite une usine de production de méthanol. L’usine a été nommée d’après Olah.
En Allemagne, il y a un projet de l’initiative Carbon2Chem de ThyssenKrupp et du ministère fédéral de l’Éducation et de la Recherche pour la production de méthanol à partir de fonderies.
Chine
Selon une étude du cabinet de conseil Methanol Market Services Asia (MMSA), la capacité mondiale devrait augmenter de 55,8 millions de tonnes en 2027, dont 38 millions serviront de carburant.
La production de méthanol en Chine repose principalement sur le charbon et doit être utilisée à la fois comme combustible à forte teneur en méthanol, tel que M85 et M100, et comme dérivé, tel que le diméthyléther. En 2007, le prix du méthanol au comptant en Chine représentait environ 40% du prix de l’essence. Les commissions d’État chinoises travaillent sur des normes nationales en matière de carburant au méthanol, tandis que les constructeurs chinois travaillent sur des moteurs au méthanol améliorés.
La capacité chinoise de production d’éther diméthylique à partir de méthanol devrait passer d’un peu moins d’un million de tonnes en 2007 à plus de six millions de tonnes. La société Sinopec souhaite à elle seule augmenter sa capacité de DME à trois millions de tonnes.