Um órgão imprimível é um dispositivo construído artificialmente projetado para a substituição de órgãos, produzido usando técnicas de impressão 3D. O objetivo principal dos órgãos imprimíveis é no transplante. Atualmente, estão sendo realizadas pesquisas sobre estruturas artificiais de coração, rins e fígado, bem como outros órgãos importantes. Para órgãos mais complicados, como o coração, construções menores, como válvulas cardíacas, também foram objeto de pesquisa. Alguns órgãos impressos estão se aproximando dos requisitos de funcionalidade para implementação clínica e incluem principalmente estruturas ocas, como a bexiga, bem como estruturas vasculares, como tubos de urina.
A impressão 3D permite a construção de camada por camada de uma estrutura de órgão particular para formar um andaime de célula. Isso pode ser seguido pelo processo de semeação de células, no qual as células de interesse são pipetadas diretamente na estrutura do andaime. Além disso, o processo de integrar células ao próprio material de impressão, em vez de realizar a semeadura depois, foi explorado.
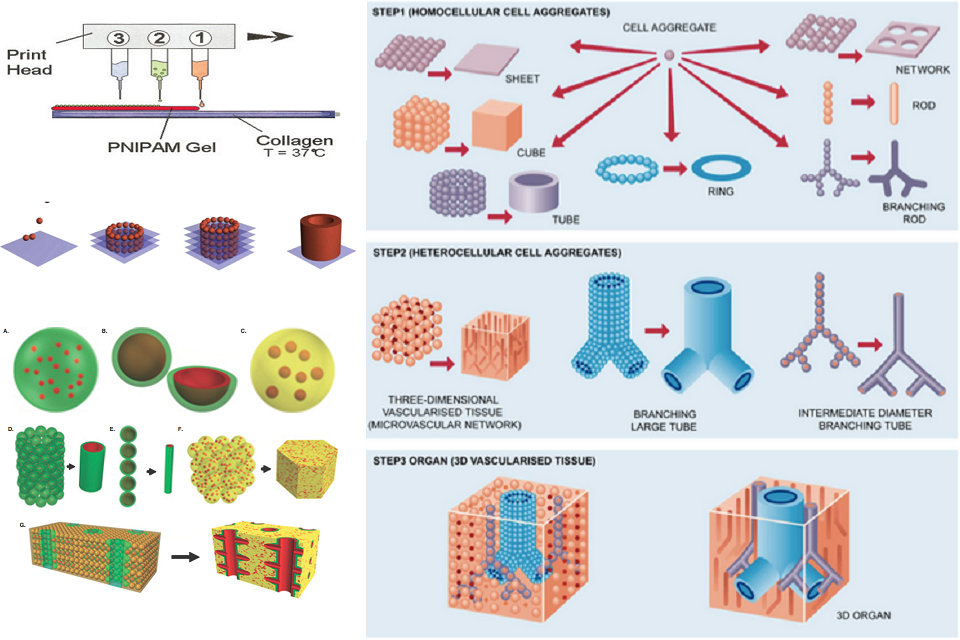
Impressoras jato de tinta modificadas têm sido usadas para produzir tecido biológico tridimensional. Cartuchos de impressora são preenchidos com uma suspensão de células vivas e um gel inteligente, o último usado para fornecer estrutura. Padrões alternados do gel inteligente e células vivas são impressos usando um bocal de impressão padrão, com as células eventualmente se fundindo para formar o tecido. Quando completado, o gel é resfriado e lavado, deixando para trás apenas as células vivas.
História
A impressão 3D para produzir uma construção celular foi introduzida pela primeira vez em 2003, quando Thomas Boland Clemson Universidade patenteou o uso da impressão a jato de tinta para células. Este processo utilizou um sistema de spotting modificado para a deposição de células em matrizes 3D organizadas colocadas em um substrato.
Desde as descobertas iniciais de Boland, a impressão 3D de estruturas biológicas, também conhecida como bioprinting, foi desenvolvida para abranger a produção de estruturas de tecidos e órgãos, ao contrário das matrizes celulares. Além disso, mais técnicas de impressão, como bioimpressão por extrusão, foram pesquisadas e subsequentemente introduzidas como meio de produção.
A impressão de órgãos tem sido abordada como uma solução potencial para a escassez global de órgãos de doadores. Os órgãos que foram impressos e implementados com sucesso em um ambiente clínico são planos, como pele, vasos vasculares, vasos sanguíneos ou ocos, como a bexiga. Quando os órgãos artificiais são preparados para o transplante, eles são frequentemente produzidos com as próprias células do receptor.
Órgãos mais complexos, nomeadamente os que consistem em estruturas celulares sólidas, estão em fase de pesquisa; Esses órgãos incluem o coração, o pâncreas e os rins. As estimativas para quando tais órgãos podem ser introduzidos como um tratamento médico viável variam. Em 2013, a empresa Organovo produziu um fígado humano usando bioimpressão 3D, embora não seja adequado para transplante, e tem sido usado principalmente como um meio para o teste de drogas.
Abordagens
Pesquisadores desenvolveram diferentes abordagens para a produção de órgãos sintéticos vivos. A bio-impressão 3D é baseada em três abordagens principais: Biomimética, auto-montagem autônoma e construção de mini blocos de tecido.
Biomimética
A primeira abordagem à bioimpressão é chamada biomimética. O principal objetivo dessa abordagem é criar estruturas idênticas às estruturas naturais. A biomimética exige a duplicação da forma, do quadro e do microambiente dos órgãos e tecidos. A aplicação da biomimética na bioimpressão envolve a cópia idêntica das partes celular e extracelular dos órgãos. Para que essa abordagem seja bem-sucedida, é necessária a replicação de tecido em escala de mícron. Este grau de precisão envolve a compreensão do microambiente, a natureza das forças biológicas, a organização precisa das células, os fatores de solubilidade e a composição e estrutura da matriz extracelular.
Auto-montagem
A segunda abordagem usada na bio-impressão é a auto-montagem autônoma. Esta abordagem baseia-se no processo físico natural de desenvolvimento de órgãos embrionários. Quando as células estão em sua fase inicial de desenvolvimento, elas criam seu próprio bloco de construção de matriz extracelular e produzem a própria sinalização da célula e tomam o layout e a microarquitetura necessários para fornecer as funções biológicas esperadas. A automontagem autônoma exige conhecimento dos processos de desenvolvimento de tecidos e órgãos no embrião. A automontagem autônoma depende das capacidades das células como o bloco de construção fundamental da histogênese. Essa técnica, portanto, requer um conhecimento muito completo dos mecanismos de desenvolvimento do tecido embrionário, bem como dos microambientes nos quais os tecidos crescem.
Mini-tecido
A terceira abordagem à bioimpressão é uma combinação de abordagens biomiméticas e de automontagem. Esta técnica é referida como “mini-tecidos”. Órgãos e tecidos são feitos de componentes funcionais muito pequenos. A abordagem do mini-tecido é pegar esses pequenos pedaços e organizá-los em uma estrutura maior. Essa abordagem usa duas estratégias diferentes. A primeira estratégia é usar esferas celulares auto-organizadas em tecidos de grande escala, usando padrões naturais como guia. A segunda estratégia é desenvolver reproduções precisas e alta qualidade de tecido e permitir que eles montem automaticamente em grandes tecidos funcionais para escalar. A mistura dessas estratégias é necessária para imprimir uma estrutura biológica tridimensional complexa.
A impressão de órgãos tem grande potencial para as tecnologias NBIC (nano, bio, info e cognitiva) promoverem procedimentos médicos e cirúrgicos, para economizar tempo, reduzir custos e criar novas oportunidades para pacientes e pacientes. profissionais de saúde.
Técnicas de impressão 3D
A impressão 3D para a fabricação de órgãos artificiais tem sido um dos principais tópicos de estudo em engenharia biológica. À medida que as técnicas de fabricação rápida exigidas pela impressão 3D tornam-se cada vez mais eficientes, sua aplicabilidade na síntese de órgãos artificiais tornou-se mais evidente. Alguns dos principais benefícios da impressão 3D residem na sua capacidade de produzir estruturas de andaimes em massa, bem como no alto grau de precisão anatômica em produtos de andaimes. Isso permite a criação de construções que se assemelhem mais efetivamente à microestrutura de um órgão natural ou estrutura de tecido.
A impressão de órgãos usando impressão 3D pode ser conduzida usando uma variedade de técnicas, cada uma das quais confere vantagens específicas que podem ser adequadas para tipos específicos de produção de órgãos. Dois dos tipos mais proeminentes de impressão de órgãos são bioimpressão por extrusão e bioprintagem por extrusão. Vários outros existem, embora não sejam tão usados ou ainda estejam em desenvolvimento.
Bioimpressão baseada em gota (jato de tinta)
Bioimpressão baseada em gota cria construções celulares usando gotículas individuais de um material designado, que muitas vezes foi combinado com uma linhagem celular. Em contato com a superfície do substrato, cada gotícula começa a polimerizar, formando uma estrutura maior à medida que gotículas individuais começam a coalescer. A polimerização é instigada pela presença de íons de cálcio no substrato, que se difundem para o bioink liquefeito e permitem a formação de um gel sólido. Bioimpressão baseada em gota é comumente usada devido à sua velocidade eficiente, embora este aspecto a torne menos adequada para estruturas de órgãos mais complicadas.
Bioimpressão por extrusão
Bioimpressão por extrusão envolve a constante deposição de um material de impressão particular e linha de células de uma extrusora, um tipo de cabeça de impressão móvel. Isso tende a ser um processo mais controlado e suave para a deposição de material ou célula, e permite que maiores densidades de células sejam usadas na construção de estruturas de órgãos ou tecidos 3D. No entanto, tais benefícios são retrocedidos pelas velocidades de impressão mais lentas impostas por esta técnica. A bioimpressão por extrusão é frequentemente associada à luz UV, que fotopolimeriza o material impresso para formar uma construção integrada mais estável.
Materiais de impressão
Os materiais para impressão 3D geralmente consistem em polímeros de alginato ou fibrina que foram integrados com moléculas de adesão celular, que suportam a fixação física das células. Tais polímeros são especificamente projetados para manter a estabilidade estrutural e ser receptivos à integração celular. O termo “bioink” tem sido usado como uma ampla classificação de materiais compatíveis com bioimpressão em 3D.
Os materiais de impressão devem atender a um amplo espectro de critérios, sendo um dos principais biocompatibilidade. Os andaimes resultantes formados por materiais impressos em 3D devem ser física e quimicamente apropriados para a proliferação celular. A biodegradabilidade é outro fator importante, e assegura que a estrutura artificialmente formada possa ser quebrada após um transplante bem-sucedido, para ser substituída por uma estrutura celular completamente natural. Devido à natureza da impressão 3D, os materiais utilizados devem ser personalizáveis e adaptáveis, sendo adequados para uma ampla gama de tipos de células e conformações estruturais.
Os alginatos de hidrogel surgiram como um dos materiais mais comumente usados na pesquisa de impressão de órgãos, pois são altamente personalizáveis e podem ser ajustados para simular certas propriedades mecânicas e biológicas características do tecido natural. A capacidade dos hidrogéis de serem adaptados às necessidades específicas permite que eles sejam usados como um material de andaime adaptável, que são adequados para uma variedade de estruturas de tecidos ou órgãos e condições fisiológicas. Um grande desafio no uso do alginato é a sua estabilidade e degradação lenta, o que dificulta a quebra do andaime de gel artificial e sua substituição pela própria matriz extracelular das células implantadas. O hidrogel de alginato que é adequado para impressão por extrusão é também menos estrutural e mecanicamente sólido; entretanto, essa questão pode ser mediada pela incorporação de outros biopolímeros, como a nanocelulose, para proporcionar maior estabilidade. As propriedades do alginato ou bio-polímero misturado são sintonizáveis e podem ser alteradas para diferentes aplicações e tipos de órgãos.
Estruturas de órgãos
Embora muitos dos desafios técnicos da impressão de órgãos sejam compartilhados com outras aplicações de bioimpressão 3D, há alguns elementos estruturais específicos de órgãos que devem ser abordados para a criação bem-sucedida de um órgão impresso transplantável.
Vascularização
A transferência de nutrientes e oxigênio para as células através de um órgão impresso é essencial para sua função. Em tecidos muito pequenos ou finos com menos de um milímetro de espessura, as células podem receber nutrientes através da difusão. No entanto, órgãos maiores requerem o transporte de nutrientes para as células mais profundas no interior do tecido, o que requer que o tecido seja vascularizado e, portanto, capaz de receber sangue para a troca de carga como oxigênio e resíduos celulares. As primeiras técnicas de estamparia de órgãos criaram tecidos sólidos que não conseguiram vascularizar, ou vascularizaram apenas lentamente à medida que os vasos sanguíneos hospedeiros entraram no transplante, levando a problemas como necrose no interior do tecido que pode ameaçar a saúde e recuperação bem-sucedida de um receptor de transplante. Técnicas desenvolvidas mais recentemente permitem que órgãos impressos sejam criados com uma estrutura 3D mais complexa, incluindo vasculatura interna preexistente, que permite uma integração mais rápida do transplante no sistema circulatório do hospedeiro. Existem várias técnicas para criar sistemas vasculares atualmente em desenvolvimento. Um método é a impressão de extrusão separada de vasos que são então incorporados em um tecido maior. Outro método é a impressão de sacrifício, na qual todo o tecido é impresso de uma vez, e um bio-solvente solúvel ou de outra forma removível é usado para formar o interior dos vasos. Uma vez que este andaime de sacrifício é removido, geralmente por um método químico ou térmico, o resto do tecido contém um padrão vascular.
Fontes celulares
A criação de um órgão completo geralmente requer a incorporação de uma variedade de diferentes tipos de células, organizadas de maneiras distintas e padronizadas. Uma vantagem dos órgãos impressos em 3D, em comparação com os transplantes tradicionais, é o potencial para usar células derivadas do paciente para formar o novo órgão. Isso diminui significativamente a probabilidade de rejeição do transplante e pode remover a necessidade de drogas imunossupressoras após o transplante, o que reduziria os riscos à saúde dos transplantes. No entanto, como nem sempre é possível coletar todos os tipos de células necessários, pode ser necessário coletar células-tronco adultas ou induzir pluripotência no tecido coletado. Isso envolve crescimento e diferenciação de células intensivos em recursos e vem com seu próprio conjunto de riscos potenciais à saúde, uma vez que a proliferação celular em um órgão impresso ocorre fora do corpo e requer a aplicação externa de fatores de crescimento. No entanto, a capacidade de alguns tecidos se auto-organizarem em estruturas diferenciadas pode fornecer uma maneira de construir simultaneamente os tecidos e formar populações celulares distintas, melhorando a eficácia e a funcionalidade da impressão de órgãos.