El efecto fotoeléctrico es la emisión de electrones u otros portadores libres cuando la luz brilla en un material. Los electrones emitidos de esta manera se pueden llamar fotoelectrones. Este fenómeno se estudia comúnmente en la física electrónica, así como en los campos de la química, como la química cuántica o la electroquímica.
De acuerdo con la teoría electromagnética clásica, este efecto se puede atribuir a la transferencia de energía de la luz a un electrón. Desde esta perspectiva, una alteración en la intensidad de la luz induciría cambios en la energía cinética de los electrones emitidos por el metal. Además, según esta teoría, se esperaría que una luz suficientemente tenue mostrara un desfase temporal entre el brillo inicial de su luz y la posterior emisión de un electrón. Sin embargo, los resultados experimentales no se correlacionaron con ninguna de las dos predicciones hechas por la teoría clásica.
En cambio, los electrones se desalojan solo por el choque de los fotones cuando esos fotones alcanzan o superan una frecuencia umbral (energía). Por debajo de ese umbral, no se emiten electrones desde el material, independientemente de la intensidad de la luz o el tiempo de exposición a la luz. (Raramente, un electrón escapará al absorber dos o más cuantos. Sin embargo, esto es extremadamente raro porque para cuando absorba suficientes cuantos para escapar, el electrón probablemente haya emitido el resto de los cuantos). Para dar sentido al hecho que la luz puede expulsar electrones incluso si su intensidad es baja, Albert Einstein propuso que un haz de luz no es una onda que se propaga a través del espacio, sino más bien una colección de paquetes de onda discreta (fotones), cada uno con energía hν. Esto arrojó luz sobre el descubrimiento previo de Max Planck de la relación de Planck (E = hν) que vincula la energía (E) y la frecuencia (ν) como derivadas de la cuantificación de la energía. El factor h se conoce como la constante de Planck.
En 1887, Heinrich Hertz descubrió que los electrodos iluminados con luz ultravioleta crean chispas eléctricas con mayor facilidad. En 1900, mientras estudiaba la radiación del cuerpo negro, el físico alemán Max Planck sugirió que la energía transportada por las ondas electromagnéticas solo podía liberarse en «paquetes» de energía. En 1905, Albert Einstein publicó un artículo que avanzaba la hipótesis de que la energía de la luz se lleva en paquetes discretos cuantificados para explicar los datos experimentales del efecto fotoeléctrico. Este modelo contribuyó al desarrollo de la mecánica cuántica. En 1914, el experimento de Millikan apoyó el modelo del efecto fotoeléctrico de Einstein.Einstein fue galardonado con el Premio Nobel en 1921 por «su descubrimiento de la ley del efecto fotoeléctrico», y Robert Millikan recibió el Premio Nobel en 1923 por «su trabajo sobre la carga eléctrica elemental y el efecto fotoeléctrico».
El efecto fotoeléctrico requiere fotones con energías que se aproximan a cero (en el caso de la afinidad electrónica negativa) a más de 1 MeV para los electrones del núcleo en elementos con un alto número atómico. La emisión de electrones de conducción a partir de metales típicos generalmente requiere unos pocos electrones-voltios, que corresponden a la luz visible o luz ultravioleta de longitud de onda corta. El estudio del efecto fotoeléctrico dio lugar a pasos importantes para comprender la naturaleza cuántica de la luz y los electrones e influyó en la formación del concepto de dualidad onda-partícula. Otros fenómenos en los que la luz afecta el movimiento de las cargas eléctricas incluyen el efecto fotoconductor (también conocido como fotoconductividad o fotoresistividad), el efecto fotovoltaico y el efecto fotoelectroquímico.
La fotoemisión puede ocurrir de cualquier material, pero es más fácilmente observable de metales u otros conductores porque el proceso produce un desequilibrio de carga, y si este desequilibrio de carga no es neutralizado por flujo de corriente (habilitado por conductividad), la barrera potencial a la emisión aumenta hasta la corriente de emisión cesa. También es habitual tener la superficie emisora en el vacío, ya que los gases impiden el flujo de fotoelectrones y dificultan su observación. Además, la barrera de energía para la foto emisión generalmente aumenta por capas delgadas de óxido en las superficies metálicas si el metal ha estado expuesto al oxígeno, por lo que la mayoría de los experimentos y dispositivos basados en el efecto fotoeléctrico utilizan superficies metálicas limpias en el vacío.
Cuando el fotoelectrón se emite en un sólido en lugar de en un vacío, el término fotoemisión interna se utiliza a menudo, y la emisión en un vacío se distingue como fotoemisión externa.
Mecanismo de emisión
Los fotones de un rayo de luz tienen una energía característica proporcional a la frecuencia de la luz. En el proceso de fotoemisión, si un electrón dentro de algún material absorbe la energía de un fotón y adquiere más energía que la función de trabajo (la energía de unión del electrón) del material, es expulsado. Si la energía del fotón es demasiado baja, el electrón no puede escapar del material. Como un aumento en la intensidad de la luz de baja frecuencia solo aumentará el número de fotones de baja energía enviados durante un intervalo de tiempo dado, este cambio en la intensidad no creará ningún fotón con suficiente energía para desalojar un electrón. Por lo tanto, la energía de los electrones emitidos no depende de la intensidad de la luz entrante, sino solo de la energía (frecuencia equivalente) de los fotones individuales. Es una interacción entre el fotón incidente y los electrones más externos.
Los electrones pueden absorber energía de los fotones cuando se irradian, pero generalmente siguen un principio de «todo o nada». Toda la energía de un fotón debe ser absorbida y utilizada para liberar un electrón de la unión atómica, o bien la energía se vuelve a emitir. Si la energía del fotón se absorbe, parte de la energía libera el electrón del átomo, y el resto contribuye a la energía cinética del electrón como una partícula libre.
Observaciones experimentales de emisión fotoeléctrica
La teoría del efecto fotoeléctrico debe explicar las observaciones experimentales de la emisión de electrones desde una superficie de metal iluminada.
Para una superficie metálica dada, existe una cierta frecuencia mínima de radiación incidente por debajo de la cual no se emiten fotoelectrones. Esta frecuencia se llama frecuencia umbral. Aumentar la frecuencia del haz incidente, manteniendo fija la cantidad de fotones incidentes (esto daría como resultado un aumento proporcional de la energía) aumenta la energía cinética máxima de los fotoelectrones emitidos. Por lo tanto, el voltaje de parada aumenta. El número de electrones también cambia debido a la probabilidad de que cada fotón resulte en un electrón emitido en función de la energía del fotón. Si se aumenta la intensidad de la radiación incidente de una frecuencia dada, no hay ningún efecto sobre la energía cinética de cada fotoelectrón.
Por encima de la frecuencia umbral, la energía cinética máxima del fotoelectrón emitido depende de la frecuencia de la luz incidente, pero es independiente de la intensidad de la luz incidente, siempre que esta última no sea demasiado alta.
Para un metal dado y la frecuencia de radiación incidente, la velocidad a la que se expulsan los fotoelectrones es directamente proporcional a la intensidad de la luz incidente. Un aumento en la intensidad del haz incidente (mantener la frecuencia fija) aumenta la magnitud de la corriente fotoeléctrica, aunque el voltaje de parada sigue siendo el mismo.
El lapso de tiempo entre la incidencia de radiación y la emisión de un fotoelectrón es muy pequeño, menos de 10-9 segundos.
La dirección de distribución de los electrones emitidos llega al máximo en la dirección de polarización (la dirección del campo eléctrico) de la luz incidente, si está polarizada linealmente.
Descripción matemática
En 1905, Einstein propuso una explicación del efecto fotoeléctrico utilizando un concepto presentado por Max Planck en el sentido de que las ondas de luz consisten en pequeños paquetes o paquetes de energía conocidos como fotones o cuantos.
La energía cinética máxima de un electrón expulsado está dado por
dónde es la constante de Planck y es la frecuencia del fotón incidente. El termino es la función de trabajo (a veces denotada , o , que proporciona la energía mínima requerida para eliminar un electrón deslocalizado de la superficie del metal. La función de trabajo satisface
dónde es la frecuencia de umbral para el metal. La energía cinética máxima de un electrón expulsado es entonces
La energía cinética es positiva, entonces debemos tener para que ocurra el efecto fotoeléctrico.
Potencial de detención
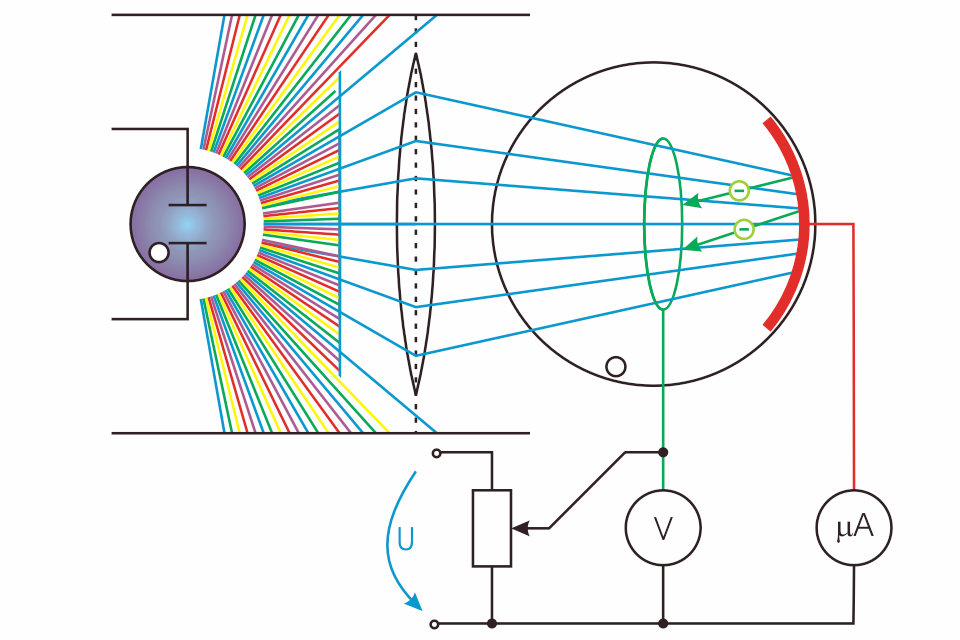
La relación entre la tensión actual y la aplicada ilustra la naturaleza del efecto fotoeléctrico. Para discusión, una fuente de luz ilumina una placa P, y otra placa electrodo Q recoge cualquier electrón emitido. Variamos el potencial entre P y Q y medimos el flujo de corriente en el circuito externo entre las dos placas.
Si se fijan la frecuencia y la intensidad de la radiación incidente, la corriente fotoeléctrica aumenta gradualmente con un aumento del potencial positivo en el electrodo colector hasta que se recogen todos los fotoelectrones emitidos. La corriente fotoeléctrica alcanza un valor de saturación y no aumenta más por ningún aumento en el potencial positivo. La corriente de saturación aumenta con el aumento de la intensidad de la luz. También aumenta con frecuencias mayores debido a una mayor probabilidad de emisión de electrones cuando ocurren colisiones con fotones de mayor energía.
Si aplicamos un potencial negativo a la placa de colector Q con respecto a la placa P y la aumentamos gradualmente, la corriente fotoeléctrica disminuye, llegando a cero con un cierto potencial negativo. El potencial negativo en el colector en el que la corriente fotoeléctrica se vuelve cero se denomina potencial de detención o potencial de corte
yo. Para una frecuencia dada de radiación incidente, el potencial de detención es independiente de su intensidad.
ii. Para una frecuencia dada de radiación incidente, el potencial de detención está determinado por la energía cinética máxima de los fotoelectrones que se emiten. Si q e es la carga en el electrón y es el potencial de detención, entonces el trabajo realizado por el potencial de retardo en detener el electrón es , entonces tenemos
Recordando
Vemos que el voltaje de parada varía linealmente con la frecuencia de la luz, pero depende del tipo de material. Para cualquier material en particular, hay una frecuencia umbral que debe excederse, independientemente de la intensidad de la luz, para observar cualquier emisión de electrones.
Modelo de tres pasos
En el régimen de rayos X, el efecto fotoeléctrico en el material cristalino a menudo se descompone en tres pasos:
Efecto fotoeléctrico interno (ver fotodiodo debajo [aclaración necesaria]). El agujero dejado atrás puede dar lugar al efecto Auger, que es visible incluso cuando el electrón no abandona el material.En sólidos moleculares, los fonones se excitan en este paso y pueden ser visibles como líneas en la energía final del electrón. El fotoefecto interno tiene que ser dipolo permitido. [Aclaración necesaria] Las reglas de transición para los átomos se traducen a través del modelo de estrecha vinculación en el cristal. [Aclaración necesaria] Son similares en geometría a las oscilaciones del plasma en que tienen que ser transversales.
Transporte balístico [se necesita aclaración] de la mitad de los electrones a la superficie. Algunos electrones están dispersos.
Los electrones escapan del material en la superficie.
En el modelo de tres pasos, un electrón puede tomar múltiples caminos a través de estos tres pasos. Todos los caminos pueden interferir en el sentido de la formulación integral de la ruta. Para los estados de superficie y las moléculas, el modelo de tres pasos todavía tiene sentido, ya que incluso la mayoría de los átomos tienen múltiples electrones que pueden dispersar el electrón que sale.
Historia
Cuando una superficie está expuesta a radiación electromagnética por encima de una determinada frecuencia umbral (típicamente luz visible para metales alcalinos, casi ultravioleta para otros metales y ultravioleta extremo para no metales), la radiación se absorbe y se emiten electrones. La luz, y especialmente la luz ultravioleta, descarga cuerpos electrificados negativamente con la producción de rayos de la misma naturaleza que los rayos catódicos. Bajo ciertas circunstancias, puede ionizar gases directamente. El primero de estos fenómenos fue descubierto por Hertz y Hallwachs en 1887. El segundo fue anunciado por primera vez por Philipp Lenard en 1900.
La luz ultravioleta para producir estos efectos se puede obtener a partir de una lámpara de arco, o quemando magnesio, o por chispa con una bobina de inducción entre terminales de zinc o cadmio, cuya luz es muy rica en rayos ultravioleta. La luz solar no es rica en rayos ultravioleta, ya que han sido absorbidos por la atmósfera y no produce un efecto tan grande como la luz de arco. Muchas sustancias, además de los metales, descargan electricidad negativa bajo la acción de la luz ultravioleta: se encontrarán listas de estas sustancias en los documentos de GC Schmidt y O. Knoblauch.
Siglo 19
En 1839, Alexandre Edmond Becquerel descubrió el efecto fotovoltaico mientras estudiaba el efecto de la luz sobre las células electrolíticas. Aunque no es equivalente al efecto fotoeléctrico, su trabajo en energía fotovoltaica fue fundamental para mostrar una fuerte relación entre la luz y las propiedades electrónicas de los materiales. En 1873, Willoughby Smith descubrió la fotoconductividad en el selenio mientras probaba el metal por sus propiedades de alta resistencia junto con su trabajo con cables de telégrafo submarino.
Johann Elster (1854-1920) y Hans Geitel (1855-1923), estudiantes en Heidelberg, desarrollaron las primeras células fotoeléctricas prácticas que podrían usarse para medir la intensidad de la luz.:458 Elster y Geitel habían investigado con gran éxito los efectos producidos por luz en cuerpos electrificados.
En 1887, Heinrich Hertz observó el efecto fotoeléctrico y la producción y recepción de ondas electromagnéticas. Publicó estas observaciones en la revista Annalen der Physik. Su receptor consistía en una bobina con una chispa, donde se vería una chispa al detectar ondas electromagnéticas. Puso el aparato en una caja oscura para ver mejor la chispa. Sin embargo, notó que la longitud máxima de chispa se redujo cuando estaba en la caja. Un panel de vidrio colocado entre la fuente de ondas electromagnéticas y el receptor absorbió radiación ultravioleta que ayudó a los electrones a saltar a través del espacio. Cuando se quita, la longitud de la chispa aumentaría. No observó una disminución en la longitud de la chispa cuando reemplazó el vidrio con cuarzo, ya que el cuarzo no absorbe la radiación UV. Hertz concluyó sus meses de investigación e informó los resultados obtenidos. Él no prosiguió la investigación de este efecto.
El descubrimiento por Hertz en 1887 de que la incidencia de la luz ultravioleta en una chispa facilitó el paso de la chispa, condujo inmediatamente a una serie de investigaciones por Hallwachs, Hoor, Righi y Stoletow sobre el efecto de la luz, y especialmente de la ultra -violeta, en cuerpos cargados.En estas investigaciones se demostró que una superficie de zinc recién limpiada, si se carga con electricidad negativa, pierde rápidamente esta carga, por pequeña que sea cuando la luz ultravioleta cae sobre la superficie; mientras que si la superficie no está cargada desde el principio, adquiere una carga positiva cuando se expone a la luz, y la electrificación negativa sale al gas por el cual está rodeado el metal; esta electrificación positiva puede aumentar mucho al dirigir un fuerte chorro de aire contra la superficie. Sin embargo, si la superficie de zinc está electrificada positivamente no sufre pérdida de carga cuando se expone a la luz: este resultado ha sido cuestionado, pero un examen muy cuidadoso del fenómeno por parte de Elster y Geitel ha demostrado que la pérdida observada en ciertas circunstancias se debe a la descarga por la luz reflejada desde la superficie de zinc de la electrificación negativa en los conductores vecinos inducida por la carga positiva, la electricidad negativa bajo la influencia del campo eléctrico que se desplaza hacia la superficie positivamente electrificada.
siglo 20
El descubrimiento de la ionización de los gases por la luz ultravioleta fue realizado por Philipp Lenard en 1900. Como el efecto se produjo a través de varios centímetros de aire e hizo muy grandes iones negativos positivos y pequeños, era natural interpretar el fenómeno, como lo hizo JJ Thomson, como un efecto de Hertz sobre las partículas sólidas o líquidas presentes en el gas.
En 1902, Lenard observó que la energía de los electrones individuales emitidos aumentaba con la frecuencia (que está relacionada con el color) de la luz.
Esto parecía estar en desacuerdo con la teoría de la luz de la onda de Maxwell, que predijo que la energía del electrón sería proporcional a la intensidad de la radiación.
Lenard observó la variación en la energía de los electrones con la frecuencia de la luz utilizando una poderosa lámpara de arco eléctrico que le permitió investigar grandes cambios en la intensidad, y que tenía suficiente poder para permitirle investigar la variación del potencial con la frecuencia de la luz. Su experimento midió directamente los potenciales, no la energía cinética de electrones: encontró la energía del electrón relacionándola con el potencial máximo de detención (voltaje) en un fototubo. Descubrió que la energía cinética de electrones máxima calculada está determinada por la frecuencia de la luz. Por ejemplo, un aumento en la frecuencia da como resultado un aumento en la energía cinética máxima calculada para un electrón tras la liberación: la radiación ultravioleta requeriría un mayor potencial de detención aplicado para detener la corriente en un fototubo que la luz azul. Sin embargo, los resultados de Lenard fueron más cualitativos que cuantitativos debido a la dificultad de realizar los experimentos: los experimentos debían realizarse en metal recién cortado para que se observara el metal puro, pero se oxidaba en cuestión de minutos incluso en los vacíos parciales usado. La corriente emitida por la superficie fue determinada por la intensidad de la luz o brillo: al duplicar la intensidad de la luz se duplicó el número de electrones emitidos desde la superficie.
Las investigaciones de Langevin y las de Eugene Bloch han demostrado que la mayor parte del efecto Lenard se debe ciertamente a este «efecto Hertz». Sin embargo, sí existe el efecto Lenard sobre el gas [aclaración necesaria]. Reconstruido por JJ Thomson y luego más decisivamente por Frederic Palmer, Jr., fue estudiado y mostró características muy diferentes a las que le atribuyó Lenard.
En 1905, Albert Einstein resolvió esta aparente paradoja describiendo la luz como compuesta de cuantos discretos, ahora llamados fotones, en lugar de ondas continuas. Basado en la teoría de la radiación de cuerpo negro de Max Planck, Einstein teorizó que la energía en cada cuanto de luz era igual a la frecuencia multiplicada por una constante, más tarde llamada constante de Planck. Un fotón por encima de una frecuencia umbral tiene la energía requerida para expulsar un solo electrón, creando el efecto observado. Este descubrimiento condujo a la revolución cuántica en física y le valió a Einstein el Premio Nobel de Física en 1921. Mediante la dualidad onda-partícula, el efecto puede analizarse puramente en términos de ondas aunque no de manera tan conveniente.
La descripción matemática de Albert Einstein de cómo el efecto fotoeléctrico fue causado por la absorción de cuantos de luz se encontraba en uno de sus documentos de 1905, llamado «En un punto de vista heurístico sobre la producción y la transformación de la luz». Este documento propuso la descripción simple de «quanta de luz», o fotones, y mostró cómo explicaban fenómenos tales como el efecto fotoeléctrico. Su explicación simple en términos de absorción de cuantos discretos de luz explica las características del fenómeno y la frecuencia característica.
El efecto fotoeléctrico ayudó a impulsar el concepto entonces emergente de la dualidad onda-partícula en la naturaleza de la luz. La luz posee simultáneamente las características de ambas ondas y partículas, cada una manifestada según las circunstancias. El efecto era imposible de entender en términos de la descripción de onda clásica de la luz, ya que la energía de los electrones emitidos no dependía de la intensidad de la radiación incidente. La teoría clásica predijo que los electrones «recogerían» energía durante un período de tiempo, y luego serían emitidos.
Usos y efectos
Fotomultiplicadores
Estos son tubos de vacío extremadamente sensibles a la luz con un fotocátodo recubierto en una parte (un extremo o lado) del interior de la envoltura. El fotocátodo contiene combinaciones de materiales como cesio, rubidio y antimonio especialmente seleccionados para proporcionar una baja función de trabajo, por lo que cuando se ilumina incluso con niveles muy bajos de luz, el fotocátodo libera fácilmente electrones. Por medio de una serie de electrodos (dinodos) a potenciales cada vez más altos, estos electrones se aceleran y se incrementan sustancialmente en número a través de una emisión secundaria para proporcionar una corriente de salida fácilmente detectable. Los fotomultiplicadores todavía se usan comúnmente donde se deben detectar bajos niveles de luz.
Sensores de imagen
Los tubos de la cámara de video en los primeros días de la televisión usaron el efecto fotoeléctrico, por ejemplo, el «disector de imagen» de Philo Farnsworth utilizó una pantalla cargada por el efecto fotoeléctrico para transformar una imagen óptica en una señal electrónica escaneada.
Electroscopio de hoja de oro
Los electroscopios de hoja de oro están diseñados para detectar electricidad estática. La carga colocada sobre la tapa de metal se extiende al tallo y la hoja de oro del electroscopio. Debido a que tienen la misma carga, el tallo y la hoja se repelen entre sí. Esto hará que la hoja se doble hacia fuera del tallo.
Un electroscopio es una herramienta importante para ilustrar el efecto fotoeléctrico. Por ejemplo, si el electroscopio está cargado negativamente por completo, hay un exceso de electrones y la hoja está separada del vástago. Si la luz de alta frecuencia brilla en la tapa, el electroscopio se descarga, y la hoja se debilitará. Esto se debe a que la frecuencia de la luz que brilla en la tapa está por encima de la frecuencia del umbral de la tapa. Los fotones en la luz tienen suficiente energía para liberar electrones de la tapa, reduciendo su carga negativa. Esto descargará un electroscopio cargado negativamente y cargará más un electroscopio positivo. Sin embargo, si la radiación electromagnética que golpea la tapa de metal no tiene una frecuencia suficientemente alta (su frecuencia está por debajo del valor límite para la tapa), entonces la hoja nunca se descargará, sin importar cuánto tiempo se ilumine la luz de baja frecuencia en el gorra.
Espectroscopia de fotoelectrones
Como la energía de los fotoelectrones emitidos es exactamente la energía del fotón incidente menos la función de trabajo del material o la energía de enlace, la función de trabajo de una muestra puede determinarse bombardeándola con una fuente de rayos X monocromática o fuente de UV y midiendo la distribución de energía cinética de los electrones emitidos.
La espectroscopía de fotoelectrones generalmente se realiza en un entorno de alto vacío, ya que los electrones se dispersarían por las moléculas de gas si estuvieran presentes. Sin embargo, algunas compañías ahora están vendiendo productos que permiten la emisión en el aire. La fuente de luz puede ser un láser, un tubo de descarga o una fuente de radiación sincrotrón.
El analizador hemisférico concéntrico es un analizador de energía de electrones típico y utiliza un campo eléctrico para cambiar las direcciones de los electrones incidentes, dependiendo de sus energías cinéticas. Para cada elemento y núcleo (orbital atómico) habrá una energía de enlace diferente. Los muchos electrones creados a partir de cada una de estas combinaciones aparecerán como picos en la salida del analizador, y estos se pueden usar para determinar la composición elemental de la muestra.
Astronave
El efecto fotoeléctrico hará que las naves espaciales expuestas a la luz solar desarrollen una carga positiva. Esto puede ser un problema importante, ya que otras partes de la nave espacial están en la sombra lo que dará como resultado que la nave espacial desarrolle una carga negativa a partir de plasmas cercanos. El desequilibrio puede descargarse a través de delicados componentes eléctricos. La carga estática creada por el efecto fotoeléctrico es autolimitada, porque un objeto cargado más alto no cede sus electrones tan fácilmente como lo hace un objeto con una carga más baja.
Polvo de luna
La luz del sol que golpea el polvo lunar hace que se cargue con el efecto fotoeléctrico. El polvo cargado se repele y se levanta de la superficie de la Luna mediante levitación electrostática. Esto se manifiesta casi como una «atmósfera de polvo», visible como una neblina delgada y borrosa de rasgos distantes, y visible como un brillo tenue después de que el sol se haya puesto. Esto fue fotografiado por primera vez por las investigaciones del programa Surveyor en la década de 1960.Se cree que las partículas más pequeñas son repelidas a kilómetros de la superficie y que las partículas se mueven en «fuentes» cuando cargan y descargan.
Dispositivos de visión nocturna
Los fotones que golpean una película delgada de metal alcalino o material semiconductor como el arseniuro de galio en un tubo intensificador de imágenes provocan la eyección de fotoelectrones debido al efecto fotoeléctrico. Estos son acelerados por un campo electrostático donde golpean una pantalla revestida de fósforo, convirtiendo los electrones en fotones. La intensificación de la señal se logra ya sea mediante la aceleración de los electrones o mediante el aumento de la cantidad de electrones a través de emisiones secundarias, como con una placa de microcanal. Algunas veces se usa una combinación de ambos métodos. Se requiere energía cinética adicional para mover un electrón fuera de la banda de conducción y dentro del nivel de vacío. Esto se conoce como la afinidad electrónica del fotocátodo y es otra barrera para la emisión de fotos que no sea la banda prohibida, explicado por el modelo de banda prohibida. Algunos materiales como el arseniuro de galio tienen una afinidad electrónica efectiva que está por debajo del nivel de la banda de conducción. En estos materiales, los electrones que se mueven hacia la banda de conducción son todos de la energía suficiente para ser emitidos por el material y, como tal, la película que absorbe los fotones puede ser bastante gruesa. Estos materiales se conocen como materiales de afinidad electrónica negativa.
Sección transversal
El efecto fotoeléctrico es un mecanismo de interacción entre fotones y átomos. Es una de las 12 interacciones teóricamente posibles.
A las altas energías de fotones comparables con la energía de reposo de electrones de 511 keV, puede tener lugar la dispersión de Compton, otro proceso. Más del doble de esta producción de par (1.022 MeV) puede tener lugar. La dispersión Compton y la producción de pares son ejemplos de otros dos mecanismos competitivos.
De hecho, incluso si el efecto fotoeléctrico es la reacción favorecida para una determinada interacción de un solo fotón con un electrón, el resultado también está sujeto a procesos estadísticos y no está garantizado, aunque el fotón ciertamente ha desaparecido y se ha excitado un electrón unido (generalmente Electrones de la cubierta K o L en energías de rayos gamma). La probabilidad de que se produzca el efecto fotoeléctrico se mide por la sección transversal de la interacción, σ. Se ha encontrado que esto es una función del número atómico del átomo objetivo y la energía del fotón. Una aproximación cruda, para energías de fotones por encima de la energía de unión atómica más alta, viene dada por:
Aquí Z es un número atómico yn es un número que varía entre 4 y 5. (A energías de fotones inferiores aparece una estructura característica con bordes, borde K, bordes L, bordes M, etc.) La interpretación obvia sigue que el efecto fotoeléctrico rápidamente disminuye la insignificancia, en la región de rayos gamma del espectro, con el aumento de la energía del fotón, y ese efecto fotoeléctrico aumenta abruptamente con el número atómico. El corolario es que los materiales de alta Z son buenos escudos de rayos gamma, que es la principal razón por la que el plomo (Z = 82) es un escudo de radiación gamma preferido y omnipresente.
 de un electrón expulsado está dado por
de un electrón expulsado está dado por








 para que ocurra el efecto fotoeléctrico.
para que ocurra el efecto fotoeléctrico.



